Ernst-Jan Eggers1,2, Ate van der Burgt1, Sjaak AW van Heusden2, Michiel E. de Vries@ 1, Richard GF Visser©2, Christian WB Bachem©2и & Pim Lindhout1
Patatesteki genetik kazanç, kültür patatesinin heterozigot tetraploid genomu tarafından engellenmektedir. Patatesin diploid kendilenmiş soy bazlı F1 hibrit mahsulüne dönüştürülmesi, artan genetik kazanıma yönelik umut verici bir yol sağlar. Baskın bir S-lokus inhibitörü (Sli) geninin diploid patates germplazmasına dahil edilmesi, kendi kendine döllenen tohumların verimli bir şekilde üretilmesine ve dolayısıyla kendi içinde melezlenmiş patates soylarının geliştirilmesine olanak tanır. Sli lokusunun yapısı ve işlevi hakkında çok az şey bilinmektedir. Burada, rekombinant tarama yaklaşımı kullanılarak Sli'nin kromozom 12.6 üzerinde 12 kb'lik bir aralığa eşlenmesini açıklıyoruz. Bu aralıkta mevcut olan iki aday genden biri, yalnızca kendi kendine uyumlu hatlarda mevcut olan benzersiz bir diziyi gösterir. Kendi kendine uyumsuz olana dönüşen bir ifade vektörünü tanımlıyoruz. genotipleri kendi kendine uyumlu ve SC genotiplerini SI'ya dönüştüren bir CRISPR-Cas9 vektörüne dönüştürülür. Sli geni, kendi kendine uyumlu bitkilerden elde edilen polenlerde spesifik olarak ifade edilen bir F-box proteinini kodlar. Bu genin promotoruna 533 bp'lik bir ekleme, kendi kendine polen reddinin üstesinden gelen fonksiyon mutasyonunun kazanılmasına yol açar.
Patates dünyadaki en önemli tahıl dışı gıda ürünüdür. Ancak mısır, pirinç ve buğday gibi diğer gıda ürünleri yılda %1 oranında genetik verim artışı gösterirken1Patateste genetik kazanç minimum düzeyde olmuştur2. Şu anda, ticari olarak yetiştirilen patates çeşitlerinin çoğu, heterozigot ototetraploid ebeveynler arasındaki melezlemelerden türetilmektedir. Bu yetiştirme sisteminde, nesilde ayrılan çok sayıda özellik için kabul edilebilir özelliklere sahip olan nadir bireylerin belirlenmesi amacıyla her yetiştirme neslinde yüzbinlerce fide üretilir ve taranır. Ticari bir patates çeşidinin değeriyle ilgili elli kadar özellik mevcut olduğundan, geleneksel patates yetiştiriciliği kullanılarak bu özellikleri kontrol eden en iyi alelleri birleştirme şansı ihmal edilebilir düzeydedir. Ek olarak, yeni özelliklerin elit çeşitlere hedefli bir şekilde dahil edilmesi ve geri melezleme şemaları yoluyla genetik bütünlüğün korunması, homozigot ebeveyn soyları olmadan mümkün değildir. Bu sorunların üstesinden gelmek için çeşitli gruplar kendilenmiş soy bazlı diploid patates yetiştirme programlarına başlamıştır.2-5. Bu programlarda, genetik kazanımlar, akrabalı yetiştirme sırasında zararlı alellere karşı sürekli seçim yaparak ve geri melezleme şemaları yoluyla kendilenmiş hatlarda faydalı alelleri istifleyerek ebeveyn soylarının kademeli olarak iyileştirilmesi yoluyla elde edilir.6. Ebeveyn kendi içinde melezlenmiş soylar daha sonra heterotik F1-hibrit yavrular üretmek için çaprazlanır.
Çoğu diploid patates genotipinde akrabalı yetiştirme, çoklu alelik S-lokusu tarafından kontrol edilen gametofitik kendi kendine uyumsuzluk (GSI) sistemi tarafından ciddi şekilde sınırlanır. Bu S lokusu, stilde kendi polen tüpünün büyümesini engelleyen ve kendi kendine döllenmeyi önleyen stil ifadeli S-RNazları kodlar7. Çapraz tozlaşma sırasında, polende eksprese edilen S-lokus F-kutusu proteinleri (SLF), S-RNazları tanır ve onları proteazomal bozunma yoluna hedefleyerek polen tüpünün döllenmenin gerçekleşebileceği yumurtalıklara doğru büyümesine izin verir.8. Her S-alel, bir S-RNaz'ı ve farklı özelliklere sahip birden fazla SLF'yi kodlar; bunlar birlikte, aynı alel üzerinde mevcut olan S-RNaz dışındaki tüm S-RNazları tanıyabilir.9.
Çoğu diploid patates hattı kendi kendine uyumsuz (SI) olmasına rağmen, kendi kendine uyumlu diploid patates hatları mevcuttur ve diploid patates yetiştirme programlarına kendi kendine uyumluluğu kazandırmak için kullanılabilir.10-12. Hosaka ve Hanneman baskın bir S-lokus inhibitörünün haritasını çıkardı (Sli) gelen gen solanum chacoense Kromozom 12'nin uzak ucundaki giriş ve bunu patates kendilenmiş hatlarını oluşturmak için kullandı13'14. Hosaka ve Hanneman, sonuçlarına dayanarak şunu önerdi: sli sporofitik aktiviteye ve homozigotluğa sahip, polenle eksprese edilen bir gendir. sli homozigot olduğundan öldürücüdür SliSli S.'nin F8 popülasyonunda genotipler yoktu. Chacoense. Bu S'lerden birini kullandık. chacoense S'ye kendi kendine uyumluluk kazandırmak için (DS) türetilmiş kendilenmiş hatlar. tüberozum arka plan. Burada, diploid patateste kendi kendine uyumluluğun biyolojisi hakkında daha fazla bilgi edinmek için kendi kendine uyumluluğun nedensel geninin tanımlanmasını açıklıyoruz.
sonuçlar ve tartışma
arasındaki çaprazlamadan elde edilen bir F2 popülasyonunda sli donör (DS olarak adlandırılmıştır) ve bir diploid S. tüberozum (D2), kromozom 2 üzerinde kendi meyve seti için mütevazı bir QTL etkisi gözlemledik, ancak daha sonraki bir rekombinant tarama başarılı olmadı. Çoklu F2 popülasyonlarının, kromozom 12'nin uzun kolu çevresinde aşırı çarpıklık gösterdiğini, DS dışı haplotip için homozigotluğun tamamen bulunmadığını fark ettik.
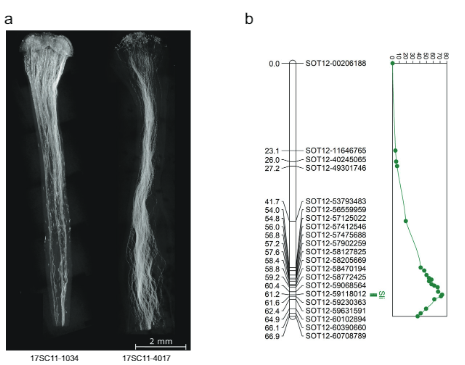
Bu çarpıklığa ve haritalamaya dayanarak sli 12. kromozomda şunu varsaydık: sli Gametofitik olarak ifade edilir, yani heterozigot bir bitkinin kendi kendine tozlaşmasında sli (Sli/sli), yalnızca baskın olanı içeren polen sli alel kendi kendine döllenmeye katılabilir. Bu hipotezi test etmek için, güçlü ve kendi kendine doğurgan bir çizgiyi (16HP1-66) güçlü, kendi kendine uyumsuz bir çizgiye (D16) geçtik, her ikisinin de tam genom dizilimini yaptık ve ortaya çıkan F1 popülasyonunu (17SC11, n = 251, Şek. 1a, b). Bu F1 popülasyonu birçok lokus için oldukça polimorfik olduğundan, doğurganlıkla ilgili olanlar da dahil olmak üzere çok çeşitli fenotipler gözlemledik. Bu nedenle, uyumluluk fenotipini karıştıran kısırlık sorunlarını önlemek için hem çapraz hem de kendi kendine tozlaşmadan elde edilen meyve ve tohum setini içeren ve ayrıca polen tüpü büyümesinin stillerde görselleştirilmesini içeren çok katı ve titiz bir fenotipleme protokolü uyguladık. Birden fazla kendi kendine meyve veren bitkiler SC olarak kabul edilirken, en az 10 kendi kendine tozlaşmadan sonra kendi kendine meyve vermeyen bitkiler, kendi kendine polen tüpü büyümesinde duraklama gösterir ve tozlaşmadan sonra toplu olarak çapraz meyveler oluşturur. polen SI olarak kabul edilir. Sonuç olarak, uyumluluk fenotipinin kesin olarak değerlendirilmesine yönelik gereklilikler karşılanmadığından popülasyonun önemli bir kısmı genetik analizlerin dışında tutuldu. Yine de, 17SC11 soyunun popülasyonunun çoğunluğunun uyumluluk durumu değerlendirilebildi ve kendi kendine uyumluluk için ayrıldığı gösterildi (Ek Veri 1). Kendi kendine uyumluluk 16HP1-66'dan kaynaklandığından, 2HP12-16'da heterozigot ancak D1'da homozigot olan kromozom 66 ve 16 üzerindeki SNP'leri hedefleyen KASP işaretleyicilerini tasarlamak için bu genotipin tüm genom dizilerini kullandık; sli anne mayozunda. Bir genetik harita oluşturduk, QTL analizi yaptık ve kromozom 75.72'nin uzun kolunda oldukça anlamlı bir QTL (LOD = 12) bulduk (Şekil XNUMX). 1b) Hosaka ve Hanneman'ın sonuçlarının doğrulanması.
QTL'yi farklı bir genetik arka planda doğrulamak için, Solynta yetiştirme programından türetilen, kendi kendine verimli başka bir genotipi SI genotipi D14 ile geçtik ve ortaya çıkan F1 popülasyonunu analiz ettik (17SC25, Ek Veri 1). 32SC17 popülasyonundaki 25 birey arasında hiçbir SI bireyi bulamadık. Ayrılan bir popülasyon oluşturmak için, en verimli genotipi seçtik ve onu 17SC11 popülasyonunda tanımladığımız iki SI genotipine geçtik, sonuçta 18SC11 ve 18SC12 popülasyonları elde edildi (Ek Veri 1 ve Ek Şekil 1). Beklendiği gibi, 18SC11 ve 18SC12 popülasyonlarının analizi, her iki popülasyonun da kendi kendine uyumluluk için ayrıldığını gösterdi. Anneyi (17SC25-8) tüm genom dizilimi için gönderdik ve bu verileri, 17SC11 popülasyonu için kullanılanla aynı yaklaşımı kullanarak yeni KASP belirteçleri tasarlamak için kullandık, ancak bu kez yalnızca kromozom 12'yi hedefledik. Sonraki QTL analizi, popülasyonda bulduğumuz QTL'yi doğruladı. 17SC11 ve 33.14SC120.94 popülasyonlarında sırasıyla 18 ve 11 LOD değerlerine sahip 18SC12 (Ek Şekil 2).
Olup olmadığını belirlemek için sli gerçekten de gametofitik olarak ifade edildiğinden, bir F2 popülasyonunu analiz ettik (19SC1, n = 160) verimli ve güçlü bir 17SC11 bireyinden türetilmiştir. Bu popülasyonda çiçeklenme ve doğurganlık F1'e kıyasla azalmıştır. Fenotipik analizde, 160 bitkiden 81'i kendi kendine uyumluydu, 78'i zayıf çiçeklenme veya zayıf doğurganlık nedeniyle belirlenmemiş (ND) olarak kategorize edildi ve bir bitki kendi kendine uyumsuz olarak puanlandı (Ek Veri 1). Ebeveynler 12HP16-1 ve D66'daki alternatif aleller için homozigot olan kromozom 16 üzerindeki SNP'leri hedef alan KASP işaretleyicileri tasarladık. Kromozom 12'nin tamamı boyunca segregasyon oranları, beklenen 1:2:1 segregasyondan önemli ölçüde sapmaktadır. Üstelik, kendi kendine uyumluluk QTL çevresinde, ebeveyn D16'nın haplotipi için homozigot lokus yoktur (Ek Şekil 3), bunun yerine heterozigot D1 / 1HP16-16: homozigot 1HP66-16 için 1: 66'lik bir ayrışma gösterir, bu da ortadan kaldırıldığını gösterir. polen eksikliği sli segregasyon distorsiyonuna neden olur. Bu, yalnızca baskın olanı taşıyan polenin olduğu hipotezini desteklemektedir. sli alel kendi kendine döllenmeye katılır. Ek olarak, bir birey dışında fenotipleme, SI ve SC arasındaki kontrast açısından kesindi ve kullanılan fenotipleme protokolünün sağlam ve neredeyse hatasız olduğunu gösterdi.
628 KB iken SLI 12SC17 popülasyonundan Sli-alelini taşıyan kromozom 11 üzerindeki aralık, 169SC18 popülasyonunda 12 KB'lik daha küçük bir örtüşme aralığına düşürüldü; bu aralıklar, Sli-genini tanımlamak için hala çok büyüktü. Bu nedenle rekombinant tarama yaklaşımıyla S/i içeren aralığı azaltmayı amaçladık. Rekombinasyona sahip bitkileri tanımlamak için sli aralıkta, proksimal kenarda iki KASP işaretçisi ve distal kenarda iki KASP işaretçisi bulunan 1374 17SC11 fidesini genotipledik. En dıştaki iki işaret arasında rekombinasyon olan 81 fide belirledik ve bunları daha ayrıntılı haritalama için seçtik. Kesin fenotipler elde etmek için bu genotipleri vejetatif olarak çoğalttık ve fenotiplemeyi genotip başına en az iki klon üzerinde gerçekleştirdik. Aralıkta daha fazla belirteç içeren 81 rekombinantı genotipledik ve aralığı beş açıklamalı gen içeren 27.37 KB'ye düşüren iki bilgilendirici rekombinant belirledik (Ek Veri 1).
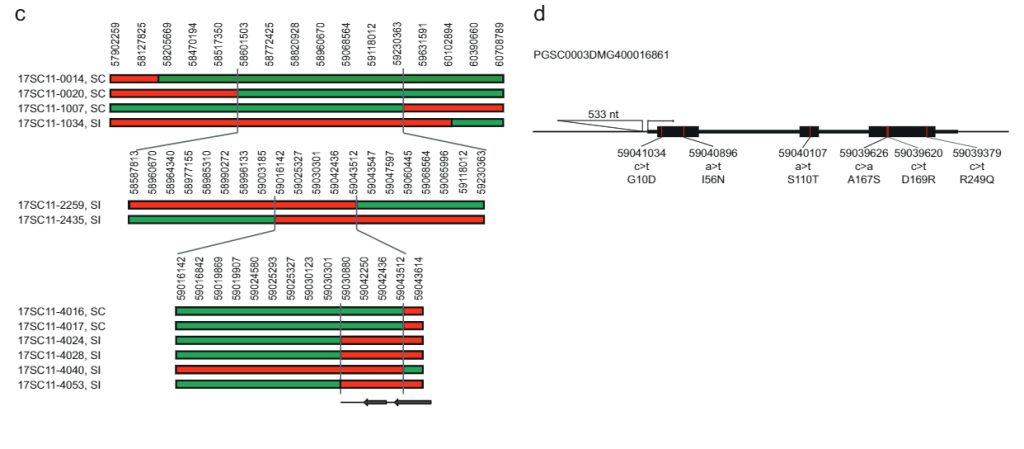
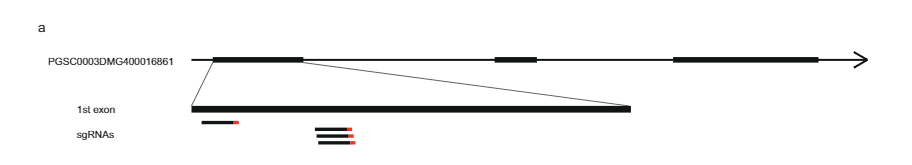
Aralığı daha da azaltmak için, aynı popülasyondan başka 10165 fideyi bu 27.37 KB aralığı etrafında dört işaretleyiciyle taradık ve 12 rekombinant belirledik. Bunlar, bu aralıkta 14 işaretleyiciyle daha genotiplendi ve net uyumluluk fenotipleri gösteren altı bilgilendirici rekombinant belirledik. SC fenotipine sahip iki rekombinant ve SI fenotipine sahip bir rekombinant, 27.37 KB aralığının distal sınırını doğrularken, SI fenotipine sahip üç rekombinant, aralığı yalnızca 12.6 kb'ye indiren, iki gen (PGSC0003DMG400016861 ve PGSC0003DMG400016860) içeren yeni bir proksimal sınır tanımladı ( İncir. 1c).
Kendi kendine uyumlu fenotipten sorumlu olan aday geni tanımlamak için, bu iki genin dizi varyasyonunu birkaç tam genom dizili diploid patates hattında analiz ettik (Ek Veri 2). Bu dizi varyasyonunu bu çizgilerin SC/SI fenotipleriyle karşılaştırarak, tüm SC'ye özgü SNP'leri ve INDELS'leri (Ek Veri 2) tanımladık. Daha sonra eşanlamlı olmayan tüm SNP'leri manuel olarak belirledik ve amino asit ikamelerinin Solanaceae'deki benzer proteinler için ortak mı yoksa benzersiz mi olduğunu belirledik. Aday gen PGSC0003DMG400016861, SC'ye özgü altı amino asit substitüsyonunu ve özellikle başlangıç kodonundan -533 bp'de bulunan 108 bp'lik bir eklemeyi gösterir; bu, SC alelinin, SI aleline kıyasla ifadeyi değiştirdiğini düşündürür. Bu genetik çalışmalara dayanarak PGSC0003DMG400016861'in sli gen.
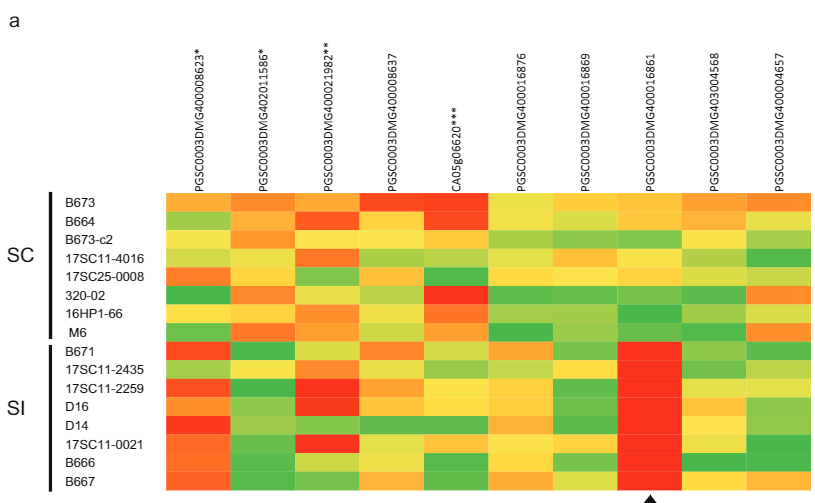
Sli'nin polende ifade edildiği hipotezini doğrulamak için, 10 SI ve 10 SC patates genotipinden poleni in vitro çimlendirdik ve RNA dizilimi için RNA'yı çıkardık. Kalan iki aday genden yalnızca aday gen PGSC0003DMG400016861 eksprese edildi, ancak yalnızca SC genotiplerinden gelen polenlerde (Şekil XNUMX). 2A). Ayrıca varsayılan aday Sli geni için heterozigot bitkilerde yalnızca Sli aleli ifade edildi. İlginç bir şekilde, Kromozom 12'deki Sli lokusuna yakın konumda bulunan diğer polen eksprese eden genler, SC ve SI bitkilerinde benzer ekspresyon seviyeleri gösterdi (Şekil XNUMX). 2A). Bu nedenle SC bitkilerinin polen tüplerinde yalnızca PGSC0003DMG400016861 geninin spesifik olarak ifade edildiği sonucuna vardık.
533 bp'lik eklemenin kökenini araştırmak için NCBI'da 533 bp'lik dizide bir BLAST araması gerçekleştirdik. İlginç bir şekilde, Sli'ye özgü eklemeye oldukça benzer diziler, sıralı S'de yaygındır. tüberozum katılımlar (Şek. 2B). Ayrıca 533 bp'lik ekleme, S'deki bir diziyle homolojiye sahiptir. Pennellii. S'deki diziyi kullanma. Pennellii BLAST sorgusu olarak S'de benzer diziler bulduk. lycopersicum. Dizilerin filogenetik analizi S. tuberosum, S. pennellii ve S. lycopersicum gruplandırır S. pennellii ile birlikte sıra S. lycopersicum ve bir S. tuberosum sekans, bunların ortak bir kökeni paylaştığını öne sürüyor (Ek Şekil 4a). Eklemenin yeri değiştirilebilen bir öğeden (TE) türetildiğini varsaydık. 533 bp'lik diziden bir nokta grafiği oluşturduk ve dizinin minyatür ters çevrilmiş tekrarlar içerdiğini gözlemledik (Ek Şekil 4b). 533 bp'lik eklemeyi tesis MITE veri tabanına karşı BLAST'a sunduk, bunun sonucunda MITE ailesinden DTA_Sot42'den birden fazla isabet elde edildi. S. tuberosum15, promotöre 533 bp'lik ekleme olduğunu gösterir sli aslında bir TE'den kaynaklanır (Ek Şekil 4c).
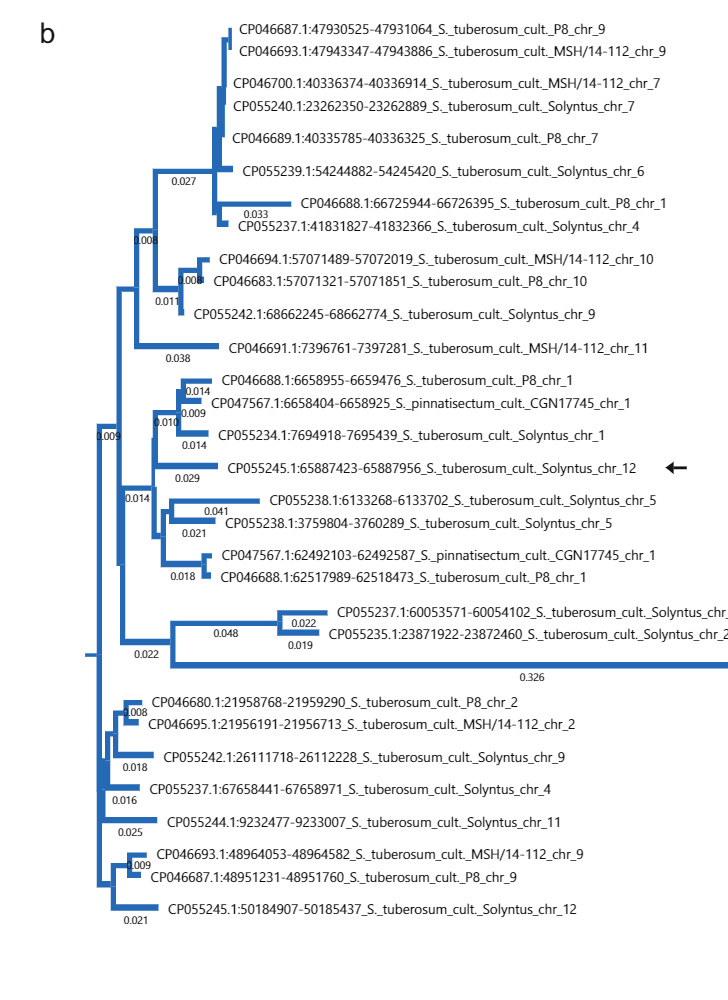
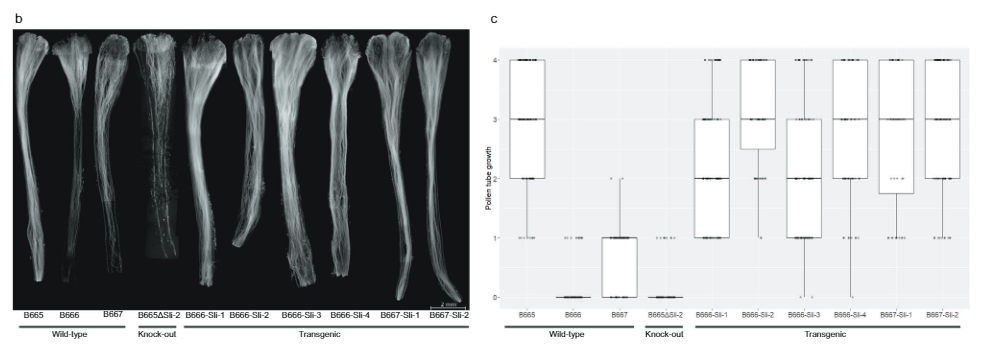
PGSC0003DMG400016861'in gerçekten olduğunu doğrulamak için sliSC allelinin eksonlarını içeren bir ifade yapısı tasarladık. sli yerli promotörü ve sonlandırıcısı arasında (Şekil 1). 3a) pBINPLUS (pBINPLUS-Sli) vektöründe. Bu yapıyı, 18SC12 popülasyonunun haritalanmasından iki SI genotipini dönüştürmek için kullandık. SI genotipi B666'dan türetilmiş beş bağımsız transgeniğin her birinden iki ila altı klonu ve SI genotipi B667'den türetilmiş üç transgeniği fenotiplendirdik.
Altı bağımsız transgenden gelen klonlar, kendi kendine tozlaşma üzerine kolayca meyveleri hazırlar (Ek Veri 3). Ek olarak, floresans mikroskobu, polenlerin sli transgenik bitkiler, dönüştürülmemiş kontrollere göre daha derin bir şekilde kendi tarzlarına doğru büyür (Şekil 1). 3M.Ö). 442 kendi kendine tozlaşmada polen tüpü büyümesini puanladık. sli 179-0 ölçeğinde dönüştürülmemiş kontrollerde transgenikler ve 4 kendi kendine tozlaşma. Çoğu durumda polen tüplerinin çoğunluğu yumurtalıklara ulaşır. sli transgenikler, kontrollerin yalnızca çok küçük bir kısmıyla karşılaştırıldığında, PGSC0003DMG400016861'in sli gen.
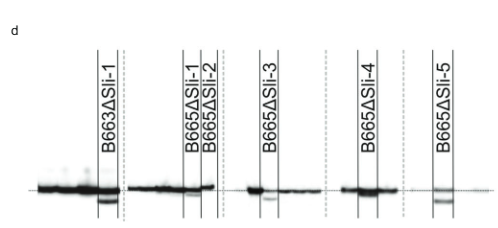
Daha sonra, PGSC9DMG0003'in ilk ekzonunu hedef alan dört gRNA'yı kodlayan bir CRISPR-Cas400016861 yapısı tasarladık (pAGM:CRISPRASli, Şekil XNUMX). 3A). Bu yapıyla iki SC genotipini (B665 ve B663) dönüştürdük ve 149 dönüştürülmüş rejenerant elde ettik. Daha sonra CRISPR-Cas9'un neden olduğu INDEL'leri tanımlamak için PAGE kullanarak hedeflenen eksonu analiz ettik. Ne yazık ki, pAGM:CRISPRASli vektörünün verimliliği düşüktü; 149 rejeneranttan yalnızca altısı INDEL'leri gösterdi. sli (İncir. 3D). Bu CRISPR-Cas9 çizgilerinden beşi INDEL'ler için heterozigottur, ancak bir çizgi, B665ASli-2, küçük bir INDEL için homozigottur. Dönüştürülmemiş B665 kolayca kendi meyvelerini oluşturur ve gözlemlenen 105 stil aracılığıyla kendi kendine polen tüpünde iyi bir büyüme gösterirken, B665ASli-2 kendi kendine tozlaşma üzerine meyve oluşturmaz ve poleni, gözlemlenen 78 stil aracılığıyla büyüyemez (Şekil XNUMX). 3b, c ve Ek Veri 3), PGSC0003DMG400016861'in gerçekten de sli gen.
S-RNaz bazlı gametofitik kendi kendine uyumsuzluk sistemlerinde, kendi kendine döllenme, polen tüplerine giren ve kendi kendine polen veya eşleşen bir S-Lokus F-kutusu (SLF) bulunmayan diğer polenler üzerinde sitotoksik etkiler uygulayan pistilde eksprese edilen S-RNazlar tarafından önlenir. ) protein. Çapraz döllenme, kendinden olmayan S-RNazları tanıyabilen ve detoksifiye edebilen, polenle ifade edilen SLF proteinleri tarafından sağlanır. Her S-alel, her biri farklı bir S-RNaz'ı tanıyabilen ve aynı S-alel üzerinde kodlanan S-RNaz dışında patateste bulunan S-RNazların çoğunu birlikte tanıyabilen birden fazla SLF'yi kodlar. Sli, bir lektin alanına bağlı bir F-box alanından oluşan bir F-box proteini PP2-B10'u kodlar. Lektin alanlarının karbonhidratlarla etkileşime girdiği bilinmektedir ve glikosile edilmiş proteinlerle etkileşime girebilmektedir.16. Ayrıca S-RNazların glikosile olduğu gösterilmiştir.17. Sli'nin SC alelinin promotörüne 533 bp'lik eklemenin, Sli'nin kendi S-RNazlarını bağlayıp detoksifiye edebildiği polende ekspresyonu mümkün kıldığını, bunun da kendi polen tüpü büyümesinin durmasına ve dolayısıyla kendi kendine uyumluluğa yol açtığını varsayıyoruz. Laimbeer tarafından patateslerdeki MITE aktivitesine ilişkin ayrıntılı bir araştırma, gen bölgelerine yakın MITE eklemelerinin %2'sinin gen ifadesindeki değişikliklerle ilişkili olduğunu buldu.
Ayrıca, gen bölgelerine yakın olan 1935'te test edilen hAT eklemelerinden 13'ü ilgili genin yukarı regülasyonuyla sonuçlandı; bu da polene özgü ifadenin değiştiğini gösteriyor. sli gerçekten de promotörüne 533 bp eklenmesinden kaynaklanabilir18. Bununla birlikte, bu hipotezin geçerliliğini belirlemek için daha fazla araştırmaya ihtiyaç vardır.
Daha önce Clot ve arkadaşları, Sli'nin bulunması gereken kromozom 333 üzerinde 12 kb'lik bir aralığı tanımlamak için toplu segregant K-mer haritalama yaklaşımını kullanmıştı.19. Burada, Sli lokusunu bir F12 popülasyonunda kromozom 1'nin aynı bölgesine haritaladık ve aralığı 12.6 gen içeren 2 KB'ye düşürmek için bir rekombinant tarama kullandık. İfade analizi, bu genlerden birinin SC alelinin, SC genotiplerinden gelen polenlerde spesifik olarak ifade edildiğini ortaya çıkardı. Son olarak, transgenik ekspresyon ve CRISPR-Cas9'un indüklediği nakavt kullanılarak, PGSC0003DMG400016861'in Sli olduğunu kesin olarak gösterdik. Laimbeer tarafından yapılan çalışma, MITE'lerin yakın genleri dokuya özgü bir şekilde yukarı doğru düzenleyebildiğini gösterse de, Sli promotöründe MITE'nin varlığının polene özgü ifadenin nedeni olduğunu kanıtlamak için daha fazla araştırmaya ihtiyaç vardır.
Bu çalışmada araştırılan materyallerde (Ek Veri 4), Sli için homozigotluk ile ilişkili öldürücülüğün daha önceki raporlarını doğrulayamadık, çünkü Sli için meyveleri ayarlayabilen homozigot canlı F2 bitkileri bulduk (Ek Veri 1)12>20. Ek olarak, kendilenmiş soy Solyntus'un ve aynı zamanda kendilenmiş M6 soyunun genom dizileri, bu iki çizginin de Sli için homozigot olduğunu gösterir; bu da Sli için homozigotluğun öldürücü olmadığını gösterir; ancak öldürücü bir mutasyonun hala mümkün olduğu söylenebilir. Bir atadaki Sli'ye genetik olarak bağlı alel, bu genotiplerde rekombinasyon yoluyla uzaklaştırılmıştır.21'22. Bununla birlikte, bu çalışmada oluşturulan verilerden, F2 popülasyonunda gözlemlenen ayrışma distorsiyonunun, Sli'nin SI aleline faz halinde bağlanan ölümcül bir alelin neden olduğu olasılığını göz ardı edemeyiz. Henüz Sli'nin kendisinin S-RNazları doğrudan tanıyıp detoksifiye edip edemeyeceği belli değil. Ayrıca Sli'nin tüm S lokus genotiplerinde kendi kendine uyumlulukla sonuçlanıp sonuçlanmadığı açık değildir. Bazı S allellerinin fonksiyonunun Sli tarafından inhibe edilememesi mümkündür. Bu soruyu çözmek için daha fazla araştırmaya ihtiyaç vardır.
Sli'nin tanımlanması, diploid patates kullanılarak kendilenmiş soy bazlı hibrit yetiştirmeyi daha da mümkün kılsa da, diğer engeller devam etmektedir. Birincisi, en önemlisi, diploid patates akrabalı yetiştirme depresyonundan muzdariptir, bu da akrabalı yetiştirme sonrasında güç ve doğurganlığın azalmasına yol açar. Diploid patates soylarının sürekli kendi kendine döllenmesi yoluyla zararlı alellerin temizlenmesi, akrabalı yetiştirme depresyonunu azaltmak için etkili bir yöntemdir ve hali hazırda nispeten güçlü ve verimli kendilenmiş patates soylarının üretilmesiyle sonuçlanmıştır.2'23-25. İkincisi, bu çalışmada kullanılan Sli donörü DS, bir S'den türetilmiştir. chacoense katılım, potansiyel olarak S'den zararlı alellerin bağlantı sürüklenmesiyle ilgili sorunlara yol açar. Chacoense. Solynta'nın diploid yetiştirme programında S. chacoense'den gelen zararlı alellerden kaynaklanan belirgin sorunlar görmüyoruz. Dahası, kendi kendine uyumluluk üzerine yakın zamanda yapılan bir çalışma, SC'ye özgü k-merlerin çeşitli tetraploid çeşitlerde zaten mevcut olduğunu ortaya çıkardı; bu, bu çeşitlerden üretilen dihaploidleri Sli donörleri olarak kullanarak bu potansiyel bağlantı sürüklemesini tamamen aşmak için bir yol sağladı.19.
Yöntemler
Bitki malzemeleri. Kullanılan tüm bitki materyalleri Ek Veri 4'te listelenmiştir.
Sera koşulları. Tüm bitkiler, sıcaklık 14°C'nin altına düştüğünde ısıtılan, sıcaklık 19°C'nin üzerine çıktığında pencereleri açılarak soğutulan seralarda yetiştirildi. Işık yoğunluğu 85 W/M2'nin altına düştüğünde yapay aydınlatma doğal ışığa destek oldu. Bitkiler, Lentse Potgrond'dan (Lentse Potgrond BV, Katwijk, Hollanda) özel bir patates substrat karışımı içinde yetiştirildi. Kullanılan substrat karışımı, dengeli su alımı için turba karışımı, temel yavaş salınımlı gübre ve gerekli pH seviyesini sağlamak için kireçten oluşur. Substrat karışımı, elektrik iletkenliği (EC) 20 olan 20:20:1.5 Nitrojen: Fosfor: Potasyum çözeltisi kullanılarak gübrelendi.
Kendi kendine uyumluluğun değerlendirilmesi. Çiçekler ve tomurcuklar haftada bir kez sayıldı ve canlılık ayda bir kez 1'den 9'a kadar bir ölçekte puanlandı; 1 son derece güçlü olmayan bir bitki ve 9 son derece güçlü bir bitkiydi. Bir bitkiden birden fazla çiçekten alınan polenler bir Eppendorf tüpünde toplandı ve haftada bitki başına maksimum 10 çiçek olacak şekilde aynı çiçekler üzerinde kendi kendine tozlaşma için hemen kullanıldı. Kendi meyvesi başına en az 35 tohum içeren ikiden fazla kendi meyvesi oluşturan bitkiler kendi kendine uyumlu olarak sınıflandırılmıştır. Dişi doğurganlığını belirlemek için bitkiler, ilgisiz en az üç genotipten gelen toplu polenlerle tozlaştırıldı. En az 10 kendi kendine tozlaşmadan sonra kendi kendine meyve vermeyen, ancak en az bir toplu meyve veren ve kendi kendine tozlaşan tarzların mikroskobik analizinde verimli polen gösteren bitkiler, kendi kendine uyumsuz olarak sınıflandırıldı. Meyve ve tohum seti verilerinin sonuçsuz kaldığı haritalama popülasyonlarından 40 genotip için (17SC11: n = 14, 18SC11: n = 7, 18SC12: n = Şekil 19), fenotipik sınıflandırma, stiller yoluyla kendi kendine polen tüpü büyümesine dayanıyordu (Ek Veri 1'de belirtilmiştir).
Stil görüntüleme. Polen tüpü büyümesini görselleştirmek için tozlaşan stiller, tozlaşmadan 24-48 saat sonra çıkarıldı ve ardından en az 3 saat boyunca 1:24 etanol:asetik asit içerisinde sabitlendi. Stiller daha sonra 8°C'de 10 dakika boyunca 65M NaOH içerisinde yumuşatıldı ve iki kez deiyonize su ile durulandı. Stiller mikroskopi slaytlarına yerleştirildi ve 2MK'de %5 Anilin mavisi (Carl Roth GmbH) kullanılarak 0.1-0.1 dakika boyunca boyandı.4P2O7 (pH = 7), daha sonra bir lamel kullanılarak gliserol içinde ezildi ve bir filtre seti 01 (BP 365/12, FT 395 ve LP 397) kullanılarak bir Zeiss Axiolab floresan mikroskobu kullanılarak gözlemlendi. Tüm stiller iki parametre kullanılarak gözlemlendi ve puanlandı: (1) maksimum penetrasyon yüzdesi olarak ifade edilen stile en derin nüfuz, (2) en derin penetrasyona ulaşan polen tüplerinin %'si. Daha sonra bu yüzdeleri 0-4 arası bir ölçeğe dönüştürdük; burada yumurtalığa hiçbir polen tüpü ulaşmayan stiller 0 puan alır, polen tüplerinin %0 ile 25 arasında olduğu stiller 1 puan alır, polen tüplerinin %25 ile 50 arasında olduğu stiller 2 puan alır, polen tüplerinin yumurtalığa ulaşmadığı stiller 50 puan alır. polen tüplerinin %75'sinin yumurtalığa ulaştığı stiller 3 puan aldı; polen tüplerinin %75 ila 4'inin yumurtalığa ulaştığı stiller XNUMX puan aldı ve polen tüplerinin %XNUMX'inden fazlasının yumurtalığa ulaştığı stiller XNUMX puan aldı. XNUMX puan.
Görüntü edinme. Seçilen stiller, Zeiss AxioCam ICc 01 kullanılarak filtre seti 5'e sahip bir Zeiss Axiophot mikroskobu kullanılarak görüntülendi. Görüntüler, Zeiss Zen 2.3 (mavi sürüm) yazılım paketi kullanılarak yapıldı. Edinme sırasında ayarlar arka planı en aza indirecek şekilde ayarlandı. Stiller, x5 objektifi kullanılarak görüntülendi ve 2464 x 2056 piksel çözünürlükte, 24 bit derinlikte TIFF dosyaları olarak kaydedildi. Daha sonra Panavue görüntü birleştirici kullanılarak sekiz adede kadar ayrı görüntü birleştirildi. Birleştirilen stillerin kontrastı ve parlaklığı, Şekil XNUMX'i oluşturacak şekilde ayarlandı. 1a ve 3c.
DNA ekstraksiyonu. Haritalama popülasyonlarının KASP analizi için yaprak örnekleri, üretici tarafından sağlanan protokole göre sbeadex™ kitleri (LGC Genomics GmbH, Berlin, Almanya) kullanılarak DNA ekstraksiyonu için VHLGenetics'e (Wageningen, Hollanda) gönderildi.
KASP analizi. Rekabetçi alel spesifik PCR (KASP™) analizi, materyalimizde ayrılan SNP'lere spesifik olacak şekilde tasarlanan KASP analizleri kullanılarak VHLGenetics (Wageningen, Hollanda) tarafından gerçekleştirildi. KASP tahlilleri, üreticinin (LGC Genomics GmbH, Berlin, Almanya) sağladığı protokole göre yapıldı. KASP analizlerinden elde edilen sonuçlar, doğru ayrışmayı ve genotip çağrısını doğrulamak için SNPviewer (lgcgroup.com/products/genotyping-software/snpviewer adresinde mevcuttur) kullanılarak görselleştirildi.
Bağlantı analizi. Kendi kendine uyumlu kadın ebeveynlerin haplotipleri, farklı SNP'ler arasındaki rekombinasyon oranları analiz edilerek genotip verilerinden yeniden yapılandırıldı. Bu veriler, SNP çağrılarını bir "axb" formatına dönüştürmek için kullanıldı; burada "a" haplotipi, Sli'nin kendi kendine uyumlu aleliyle bağlantılıyken, "b" haplotipi, Sli'nin kendi kendine uyumsuz bir aleliyle bağlantılıdır. Bağlantı haritaları, joinmap 4.1 kullanılarak oluşturuldu26 DH popülasyon türü ve varsayılan ayarlarla.
QTL eşlemesi. Fenotip verileri, kendine uyumlu her genotipe 1, kendine uyumsuz her genotipe 0 ve uyumluluğu belirlenemeyen genotiplere * atanarak sayısal bir özelliğe dönüştürüldü. QTL eşlemesi, MapQTL'deki aralık eşlemesi kullanılarak gerçekleştirildi27. MapQTL çıktıları, Mapchart 2.3 ile QTL grafikleri oluşturmak için kullanıldı28.
Biyoinformatik analiz. İlk 27.37 kb aralığında doğru gen modellerini belirlemek için DM4.04 referans genomu için iki ayrı gen açıklamasını, PGSC açıklamasını ve ITAG açıklamasını araştırdık. Ayrıca bkz. Hirsch ve diğerleri.29. Ek açıklamaların doğruluğunu doğrulamak için her iki ek açıklamadan tahmin edilen protein dizileriyle BLASTp aramaları yaptık. BLASTp aramasındaki en iyi sonuçları sorgumuzla karşılaştırarak, tahmin edilen protein dizisindeki tüm açıklamalı eksonların ve alanların patates ve diğer bitki türlerindeki benzer proteinler tarafından desteklenip desteklenmediğini belirledik. Ayrıca, SPUD DB'de (solanaceae.plantbiology.msu.edu/cgi-bin/gbrowse/potato/ adresinde mevcuttur) ve NCBI genom veri görüntüleyicisinde (ncbi.nlm.nih.gov/ genome/gdv adresinde mevcuttur) halka açık RNA dizilimi kitaplıkları /browser/) varsayılan eksonların ifade kanıtı olup olmadığını belirlemek için kullanıldı. Bu iki yaklaşım birlikte, her iki açıklamadaki gen modellerinin intron-ekson yapılarını doğrulamamıza olanak tanıdı ve bu da söz konusu geni temsil edecek gen modellerinin bir veya daha fazla izoformu için bilinçli bir seçim yapılmasına yol açtı. Bu yaklaşımlara dayanarak, aday gen PGSC0003DMG400016862'nin muhtemelen kısmi ve önemsiz düzeyde eksprese edildiği kabul edildi ve daha sonraki analizlerden çıkarıldı. Sotub12g029970 gen modeli doğru kabul edilirken, PGSC muadili PGSC0003DMG400016860 muhtemelen kesilmiştir. Büyük ölçüde belirlenen aralığın dışında yer aldığından ve SC ve SI bitkileri arasında ilgili amino asit ikameleri tanımlanamadığından, bu gen daha sonraki analizlerden çıkarıldı.
Varyasyon analizi. Kendi kendine uyumlu genotiplere özgü 27.37 kb aralığındaki mutasyonları tanımlamak için, (3) DS, 1SC17-100 ve 18SC17-100'de homozigot olan tüm yüksek güvenirli SNP'ler (Ek Veri 2) belirlendi (çünkü üçü de homozigottur) SC aleli Sli (Sli/Sli')'), (2) D16'da farklı homozigot (çünkü D16, Sli'nin SI aleli için homozigottur (sli/sli)) ve (3) hem 16HP1-66 hem de 17SC25-8'de heterozigot (çünkü her ikisi de SC aleli Sli (Sli) için heterozigottur) /sli)). Alelik dizi, SPAdes versiyon 3.11.1 kullanılarak de novo birleştirme yoluyla elde edildi.30 Yukarıda listelenen bitkilerin 150 nt çift uçlu Illumina verileri (yaklaşık 25-30X sıralama derinliği). Ortaya çıkan bitişiklikler DM referansına göre hizalandı (minimap2 sürüm 2.1 kullanılarak) ve 27 kb'ye güvenilir şekilde hizalananlar için filtrelendi. Bu hizalanmış bitişiklerden, DM4.03'e göre varyasyon doğrudan ölçüldü (mpileup ve bcftools, sürüm 1.9'dan çağrı alt yordamları kullanılarak) ve Varyant Çağrı Formatında (VCF) listelendi.
Amino asit değişim analizi. SC'ye özgü mutasyonların bu listesinden, eşanlamlı olmayan tüm SNP'ler, belirlenen kodlama ekzonlarıyla örtüşerek tanımlandı. DM veya SI sekansına göre amino asit değişiklikleri listelendi. Benzersiz amino asit değişiklikleri, protein dizisini kullanarak BLASTp aramaları gerçekleştirilerek ve ilk 100 BLASTp isabeti kullanılarak çoklu dizi hizalaması gerçekleştirilerek belirlendi.
Promoter ve sonlandırıcı bölgelerdeki varyasyon. Promotör bölgesi, maksimum 1500 nt'lik üst genin kodlama dizisine kadar başlangıç kodonunun yukarı akış dizisi olacak şekilde seçildi. 27.37 kb aralığında promotör bölgelerde dramatik varyasyon bulundu; bunların en dikkat çekici olanı, onlarca ila yüzlerce nükleotit uzunluğundaki birkaç büyük silme ve eklemeydi. DM'ye göre Sli aralığındaki tüm değişiklikler, promotor/yukarı akış bölgesinin yanı sıra sonlandırıcı/aşağı akış bölgesi de dahil olmak üzere elde edildi.
Polen edinimi ve çimlenmesi. Şekil 2'de listelenen genotiplerden polenler. 2a, açık çiçeklerin elektronik bir diş fırçası kullanılarak titreştirilmesi ve polenin 1.5 ml'lik Eppendorf tüplerinde toplanmasıyla elde edildi. Satın alma işleminden sonra polen, açık Eppendorf tüplerinin polenle birlikte silika jel içeren hava geçirmez bir kutuda oda sıcaklığında 24 saat saklanmasıyla kurutuldu. Daha sonra polen bir sonraki kullanıma kadar -20°C'de saklandı.
Polen, 2.5 mg kurutulmuş polenin 5 ml sıvı ortamda (%9 (a/h) sakaroz, 50 mg/l Borik asit, 73.5 mg/l CaCly2H) süspanse edilmesiyle çimlendirildi.2O, 118 mg/l Ca (NO3)24 saat2O, 123 mg/l MgSO.4VH2O) 3.5 cm çapındaki Petri kaplarına parafilm ile kapatılmıştır. Polen, oda sıcaklığında ve 24 RPM'de çalkalanan bir çalkalama inkübatöründe karanlıkta 125 saat boyunca Petri kaplarında çimlenmeye bırakıldı. Çimlenmiş poleni içeren sıvı ortam daha sonra polen tüplerine zarar vermeyecek şekilde açıklık boyutunu artıracak şekilde değiştirilmiş pipet uçları kullanılarak 2 ml'lik Eppendorf tüplerine dikkatlice pipetlendi. Eppendorf tüpleri daha sonra 600xg'de 1 dakika boyunca santrifüjlendi ve ortam pipetleme yoluyla dikkatlice çıkarıldı. Pelet ve kalan ortamın bir kısmı daha sonra hemen sıvı nitrojen içerisinde donduruldu, iki paslanmaz çelik boncuk (2 mm çapında) ilave edildi ve numuneler, 20 dakika boyunca 1 Hz'de bir TissueLyser II (Qiagen GmbH, Hilden, Almanya) kullanılarak öğütüldü.
RNA ekstraksiyonu ve dizileme. Öğütülmüş polen örneklerine tampon RLT (Qiagen GmbH) eklendi ve örneklerin donmuş halde kalması sağlandı. Daha sonra üreticinin protokolüne (Qiagen GmbH, Hilden, Almanya) göre RNeasy mini kiti kullanılarak RNA ekstraksiyonu gerçekleştirildi. 250-300 bp'lik ekleme boyutundaki cDNA kitaplıkları, 150nt çift uçlu okumalar olarak dizildi; örnek başına 30-42 milyon okuma çifti elde edildi (Novogene, Cambridge, Birleşik Krallık).
Diğer RNA-seq veri setleri. (Dokuya özgü) ekspresyon düzeylerine genel bir bakış oluşturmak için, ORGANİZMA olarak etiketlenen tüm çift uçlu dizili RNA dizisi veri setleri “Sola-num tuberosum” kamuya açık alandan indirildi (NCBI-SRA, tarih 2018/17/13), toplam 441 eşleştirilmiş fastq veri seti. Bu 441 halka açık veri setinden 3'ü stil dokusundan (SRR7402817-SRR7402819) ve diğerleri çeşitli polen olmayan dokulardan, gelişim aşamalarından ve bitki türlerinden üretildi.
Solyntus referans düzeneği. İfade analizleri için, yakın zamanda elde edilen homozigot referans çizgisi Solyntus'un taslak derlemesi (versiyon 1.0, şu adresten indirilebilir: www.plantbreeding.wur.nl/Solyntus/) referans genomu olarak kullanıldı. Solyntus, Solynta'nın yetiştirme programının bir parçası olarak üretilen, esas itibarıyla homozigot bir çeşittir.21. Bu çalışmadaki haritalama aralıkları DM v4.03 genom düzeneğinden çıkarılmıştır.31 (Solyntus 1.0 genom derleme koordinatları) 1.0-53532708 (Aralık I, 53954293kb < —421.6kb), 628.9-53683239 (Aralık II, 53867377) konumunda bulunacak temel benzerlik aramalarıyla (BLASTn ve bedtools kullanılarak) Solyntus 184.1 genom derlemesine kb< — 168.7kb), 53731620-53763003 (Aralık III, 31.4kb< —27.4kb) ve 53753977-53763003 (Aralık IV, 9.0kb < —12.6 kb). Parantezlerin arasında sırasıyla ardışık eşleme aralığı numarası [Solyntus 1.0 koordinatları], Solyntus-1.0'da boyut ve DM-4.03/4.04'te boyut vardır. Tüm aralıklar ST4.03ch12_RaGOO kromozomu üzerinde bulunur (kromozom 12'dir) ve Solyntus 1.0 düzeneğinde tek bir boşluk içermez. Aralık boyutu varyasyonuna, karşılık gelen DM sekansındaki çok sayıda boşluk (N'ler) ve her iki genom arasındaki kapsamlı varyasyon neden olur. DM genomunda karşılık gelen aralıklar (DM-4.03/4.04): Aralık I: chr12:58601503-59230363, Aralık II: chr12:58962004-59130723; Aralık III: 59016142-59043512; Aralık IV: chr12:59030880-59043512.
Solyntus 1.0'daki gen açıklaması, üç farklı gen kataloğundan (patates DM4.03, ITAG4.0 Domates Genomu Açıklama Sürümü, 6 Eylül 2019) çıkarılmıştır.32ve Pepper-v. 1.5533), GeMoMa (v1.6.1) kullanılarak Solytus düzeneğine eşlendi. Bu, bireysel gen kataloglarındaki kusurları telafi etmek ve olası genlerin ve/veya ifade edilen lokusların varlığına ilişkin farkındalığımızı en üst düzeye çıkarmak için yapıldı.
RNA-seq okuma haritalaması ve transkript bolluğu miktarıfikatyon. 5 SC, 3 SI ve 441 genel RNA-seq veri setinin tümü, hisat2 (versiyon 2.1.0) kullanılarak Solyntus referans genomuyla eşlendi. GeMoMa kullanılarak elde edilen hibrit gen kataloğu, -t -c 2.1.1 -f 5 -G ayarları ve bir GeMoMa birleştirilmiş Solyntus0.05 gff dosyası ile StringTie (versiyon 1.0) kullanılarak transkript rehberli bolluk tahmini için kullanıldı. Çevresini çevreleyen 500 kb'lik bir aralıkta gözlemlenen tüm ifadeler sli Lokus bir merkez olarak değerlendirildi ve bu aralıkta toplam 90 (çıkarılan) gen lokusunun yer aldığı görüldü. Bu gen lokuslarının herhangi birinin dışındaki SC örneklerinde gözle görülür herhangi bir ifadenin bulunmadığını doğruladık. 500 kb aralığında, yukarıda tanımlandığı gibi haritalama aralıklarımız I-IV ile kesişirken daha sonra daha az sayıda aday gen gösterdik.
ilefihaplotip spesifik oluşumufic ifadesi. 90 kb aralığında eksprese edilen 500 lokustan yalnızca 8'i, tüm SC/SI numunelerinde seçilen 20 FPKM eşiğinin üzerinde eksprese edildi. Bu siteleri haplotipe özgü (Sli veya sli) ifade düzeyi farklılıklarını ölçmek için kullandık. Seçilen ifade eşiği, ifadenin sonunda ve güvenilir bir şekilde (en fazla) 2 haplotip halinde aşamalandırılması için yeterli okuma derinliğini mümkün kıldı. PSC lokusunun kendisiyle (SI bitkilerinde ekspresyonu bulunmayan) birlikte bu 8 + 1 lokus, 8 numunenin her birinde haplotiplendi (SAMtools faz versiyon 1.7, varsayılan ayarlar). Ortaya çıkan haplotiplenmiş (eşleştirilmiş) fastq dosyaları, SPAde'ler (versiyon 3.11.1) kullanılarak de novo birleştirildi. Ortaya çıkan kontigler bolluk açısından filtrelendi ve ana (haplotiplenmiş) ifade edilen izoforma karşılık gelen tam uzunlukta mRNA'lar olduğu varsayıldı. Bazı durumlarda bu, alternatif olarak birleştirilmiş izoformları ortadan kaldırdı; bunların hiçbiri, belirgin bir biyolojik öneme sahip olacak şekilde geniş okumalarla desteklenmedi. Bu haplotiplenmiş mRNA dizilerindeki varyasyon, karşılık gelen lokusların/örneklerin her birinde bir veya her iki haplotipin ifade edilip edilmediğini doğrulamak/doğrulamamak için kullanıldı.
Tasarımı sli ifade yapısı. Sli ekspresyon kasetini tasarlamak için Sli donör tesisi DS'nin dizisini kullandık. Yerel ifadeye izin vermek için PSC, doğal promotörü (başlangıç kodonunun 1563 bp yukarısında), üç eksonu ve doğal sonlandırıcıyı (durdurma kodonunun 740 bp aşağısında) içeren bir nükleik asit dizisi oluşturduk. Böylece her iki intron da uzaklaştırıldı. PSC donör bitki DS geni. Bu sekans Genscript (Genscript Biotech, Leiden, Hollanda) tarafından sentezlendi ve pBINPLUS'a klonlandı. içeren vektöre atıfta bulunuyoruz. sli pBINPLUS-Sli olarak takın.
CRISPR'ın inşası-Cas9 vektörü. SC ve SI alelleri arasında hiçbir varyasyonun bulunmadığı konumlarda DM0003'teki PGSC400016861DMG4.03 dizisine dayalı olarak dört gRNA tasarladık. Uygun kılavuzların seçimi ve vektörün oluşturulması için Santillan Martinez ve diğerleri tarafından açıklanan yöntemi kullandık.34. Kısaca, Liang ve arkadaşları tarafından açıklanan yönergelere göre dört sgRNA seçildi.35. CC-Top CRISPR/Cas9 hedef tahmin aracı, sgRNA'ların bir listesini oluşturmak için kullanıldı36, katlama Mfold web sunucusu kullanılarak değerlendirildi37ve sgRNA'ların aktivitesi, sgRNA puanlayıcı kullanılarak tahmin edildi38. Aşağıdaki kılavuzlar seçilmiş ve pAGM:CRISPRASli vektörünü oluşturmak için kullanılmıştır: exon5.1T01 (ATTTCATCCGCGATCTCTCGGGG), exon5.1T04 (GATTTCA TCCGCGATCTCTCGGG), exon5.1T06 (TATTTCCTATTGCTACCAGAAGG) ve exon5.1T07 (TGATTTCATCCGCGATCTCTCGG). CRISPR yapısı daha sonra Addgene'den elde edilen plazmidler kullanılarak sentezlendi: pICH86966 (amplifikasyon şablonu); pICSL01009 (seviye 0 plazmid); pICH47751, pICH47761, pICH47772, pICH47781 ve pICH47732 (seviye 1 plazmidler); pICH41822 (dört kılavuz için bağlayıcı); ve pAGM4723 (seviye 2 ikili vektör). Plazmit kullanılarak klonlandı E. coli DH5a ve saflaştırılmış plazmid, tüm bileşenlerin (NPTII, Cas5843 ve sgRNA'lar) varlığını ve doğru yönelimini doğrulamak için PDS8535 (TTTGTGATGCTCGTCAGGGGG), PDS8536 (CCCGAGAATTATGCAGCATT TT) PDS717 (TCATCAGTCAATTACGGGGCT) ve AL9 (GCTTGGCATC AGACAAACCGG) primerleri kullanılarak sekanslama için gönderildi.
pBINPLUS-Sli ve pAGMzCRISPR'nin dönüşümüAKaydırma vektörü Agrobacterium tumefaciens. pBINPLUS-Sli'yi şuna dönüştürdük: A. tumefaciens AGL0 ve pAGM:CRISPRASli'yi A'ya süzün. Tumefaciens bir elektroporasyon protokolü kullanılarak AGL0 ve AGL1 suşları. 40 ul yetkin AGL0 hücresi aldık ve 110 ul buz soğukluğunda milliQ su ekledik. Bu karışımın 50 ul'sini buz üzerinde önceden soğutulmuş Eppendorf tüplerine pipetledik ve 1 ul plazmid ekledik. Hücreleri 15 dakika boyunca buz üzerinde bıraktık ve hücreleri önceden soğutulmuş elektroporasyon küvetlerine aktardık. Karışımları bir Micropulser™ (Bio-Rad Laboratories, Vee-nendaal, Hollanda) ile Ec1 programını (1.8 kV, 0.1 cm küvet) kullanarak elektroporasyona tabi tuttuk. 1 ml LB ekledik ve hücreleri bir çalkalayıcı üzerinde 3°C ve 28 RPM'de 200 saat süreyle inkübe ettik. Daha sonra Rifampisin (100 pg/ml) ve Kanamisin (50 pg/ml) içeren LB agar plakalarını transformasyon kültürüyle aşıladık. Seçilen tüm kolonilerin doğru vektörü içerdiği doğrulandı.
Patates genotiplerinin dönüşümü. Visser tarafından açıklanan kök eksplant yöntemini kullanarak B666 ve B667 genotiplerini pBINPLUS-Sli ile ve B663 ve B665 genotiplerini pAGM:CRISPRASli vektörüyle dönüştürdük.39. Kısaca, in vitro olarak yetiştirilen genotiplerden boğum arası eksplantlar elde edildi ve 3 ml PACM ortamı ile R2B ortamı içeren Petri kaplarına yerleştirildi. Ertesi gün 50 saatte 48 ml agrobakteri kültürler santrifüjlendi ve 75 ml LB içerisinde yeniden süspanse edildi. Boğum arası eksplantlar daha sonra suya batırıldı. agrobakteri 5 dakika boyunca süspansiyon, filtre üzerinde kurutuldu ve R3B ortamını içeren Petri kaplarına geri yerleştirildi. 48 saatlik inkübasyonun ardından eksplantlar, antibiyotiklerle birlikte MS20 içeren Petri kaplarına aktarıldı ve sürgünlerin yenilenmesine izin vermek için bir büyüme odasına yerleştirildi. Rejenerasyondan sonra sürgünler, sefotaksim (20 pg/ml), vankomisin (200 pg/ml) ve kanamisin (200 pg/ml) içeren MS100 ortamı üzerinde büyütüldü. Sürgünler yeterli uzunluğa ulaştığında kesimler yapıldı ve antibiyotiksiz MS20'de büyütüldü. Antibiyotiksiz MS20 üzerinde en az iki hafta büyütüldükten sonra bitkiler seraya dikildi.
Ploidi analizi. Transgenik bitkilerin ve dönüştürülmemiş kontrollerin ploidisi, Plant Cytometry Services (Didam, Hollanda) tarafından akış sitometrisi kullanılarak belirlendi. Tetraploid rejenerantların tümü atıldı.
CRISPR'ın PAGE analizi-Cas9 kaynaklı mutasyonlar. DNA ekstraksiyonu, PCR ve PAGE analizi Limgroup (Horst, Hollanda) tarafından gerçekleştirildi. CRISPR-Cas9 hedefli bölgeyi amplifiye etmek için aşağıdaki primerler kullanıldı: İleri primer: CTATTTCCTATTGCTACCAG, ters primer: AAACTTTACCCAAAT AACGTC. PCR ürünlerinin etiketlenmesi, M13 kuyruklu bir ters primerin (primer dizisi: TGTAAAACGACGGCCAGTAAACTTTAC CCAAATAACGTC) ve 700 IRDye veya 800 IRDye etiketli M13 primerinin PCR karışımına eklenmesiyle sağlandı. Ortaya çıkan PCR ürünleri, bir Li-cor sistemi kullanılarak PAGE'de analiz edildi. CRISPR-Cas9'un neden olduğu mutasyonları olmayan çoğu çizgiden PCR ürünleri, Şekil XNUMX'i oluşturmak için jel görüntülerinden çıkarıldı. 3d (kesikli çizgilerle gösterilen eksizyonlar).
533 bp'lik eklemenin filogenetik analizi. 533 bp'lik eklemenin sırası, NCBI web sitesindeki BLASTn kullanılarak analiz edildi. Mevcut ekleme de dahil olmak üzere en iyi 30 sonuç sli Solyntus'ta indirildi ve varsayılan ayarlarla MUSCLE kullanılarak MegAlign Pro 17'de (DNASTAR) hizalandı. Ağaçlar, varsayılan ayarlarla komşu birleştirme algoritması kullanılarak oluşturuldu.
Raporlama özeti. Araştırma tasarımına ilişkin daha fazla bilgiyi bu makaleyle bağlantılı Doğa Araştırma Raporlama Özeti'nde bulabilirsiniz.
Veri kullanılabilirliği
Solyntus genom dizisi ve ham dizi okumaları, katılım kapsamında NCBI'de mevcuttur PRJNA631911. Solyntus genom derlemesi ve açıklama dosyaları WUR'dan temin edilebilir [https://www.plantbreeding.wur.nl/Solyntus/] Çimlenmiş polenden elde edilen RNA dizileme verileri, katılım aşamasındaki NCBI kısa okuma arşivinde mevcuttur. PRJNA713577. Diğer veriler kaynak veri dosyasında mevcuttur veya talep üzerine sağlanacaktır. Kaynak veriler bu yazıyla birlikte verilmektedir.
Alınma tarihi: 22 Ocak 2021; Kabul tarihi: 8 Haziran 2021;
Referanslar
- 1. Duvick, DN Mısırda (Zea) verim artışına ıslahın katkısı mays L.). Av. Agron. 8683-145 (2005).
- 2. Lindhout, P. ve diğerleri. F1 hibrit tohumluk patates yetiştiriciliğine doğru. Patates Res. 54301-312 (2011).
- 3. Jansky, SH ve diğerleri. Patatesin diploid soy bazlı bir ürün olarak yeniden keşfedilmesi. Mahsul Bilimi. 561412-1422 (2016).
- 4. Ye, M. ve ark. S-RNaz'ın devre dışı bırakılmasıyla kendi kendine uyumlu diploid patatesin üretilmesi. Nat. Bitkiler 4651-654 (2018).
- 5. Enciso-Rodriguez, F. ve diğerleri. CRISPR-cas9 kullanarak diploid patateste kendi kendine uyumsuzluğun üstesinden gelinmesi Ön. Plant Sci. 101-12 (2019).
- 6. Su, Y. ve ark. Karşı direnç için genlerin introgresyonu Fitoftora infestans diploid patateste. Am. J. Patates Arş. 9733-42 (2020).
- 7. Dzidzienyo, DK, Bryan, GJ, Wilde, G. & Robbins, TP Diploid patates türlerinde S-RNaz alellerinin alelik çeşitliliği. Teori. Başvuru Genet. 1291985-2001 (2016).
- 8. McClure, B., Cruz-Garcia, F. & Romero, C. S-RNaz bazlı sistemlerde uyumluluk ve uyumsuzluk. Anne. Bot. 108647-658 (2011).
- 9. Kubo, K. ve diğerleri. S-RNase tabanlı kendi kendine uyumsuzlukta işbirlikçi, kendini tanımayan sistem. Bilim 330796-799 (2010).
- 10. De Jong, H. & Rowe, PR Ekili diploid patateslerde akraba yetiştirme. Patates Res. 1474-83 (1971).
- 11. Hermsen, JGT & Olsder, J. Dihaploidlerde kendi kendine uyumluluğun genetiği Solanum tuberosum L. 1. Kendi kendine uyumlu iki dihaploidin üreme davranışı. öphytica 25597-607 (1976).
- 12. Hosaka, K. & Hanneman, RE Jr. Kendi kendine uyumsuz yabani diploid patates türlerinde kendi kendine uyumluluğun genetiği solanum chacoense. 1. Bir S lokus inhibitörü (Sli) geninin saptanması. öphytica 99191-197 (1998).
- 13. Hosaka, K. & Hanneman, RE Jr. Kendi kendine uyumsuz yabani diploid patates türlerinde kendi kendine uyumluluğun genetiği solanum chacoense. 2. DNA işaretleyicileri kullanılarak patates genomu üzerindeki bir S lokus inhibitörü (Sli) geninin lokalizasyonu. öphytica 103265-271 (1998).
- 14. Birhman, RK & Hosaka, K. Bir S-lokus inhibitörü (Sli) geni kullanılarak kendi içinde melezlenmiş diploid patates nesillerinin üretimi ve bunların karakterizasyonu. Genom 502495-502 (2000).
- 15. Chen, J., Hu, Q., Zhang, Y., Lu, C. & Kuang, H. P-MITE: bitki minyatür ters çevrilmiş tekrarlanabilir öğeler için bir veritabanı. Nükleik Asitler Arş. 421176-1181 (2014).
- 16. Stefanowicz, K., Lannoo, N. ve Van Damme, EJM Bitki F-kutusu proteinleri— yaşam ve ölüm arasında karar verir. Kritik. Rev. Bitki Bilimi. 34523-552 (2015).
- 17. Liu, B., Morse, D. & Cappadocia, M. S-RNazların glikosilasyonu, Solanum chacoense'deki polen reddi eşiklerini etkileyebilir. J. Uzm. Bot. 59545-552 (2008).
- 18. Laimbeer, FPE Patates genomiğinin üç yolu vardır: Yumrularda endoreduplikasyonun miktarının belirlenmesi, transpozon alanında bir boğuşma ve çiçek rengi düzenlemesinin aydınlatılması. http://hdl.handle.net/10919/84480 (2018).
- 19. Clot, CR ve diğerleri. Patateste Sli bazlı kendi kendine uyumluluğun kökeni ve yaygın oluşumu. Teori. Başvuru Genet. https://doi.org/10.1007/s00122-020-03627-8 (2020).
- 20. Endelman, J., Jansky, SH, Butler, N. & Christensen, G. Amerika Patates Derneği'nin 12 yıllık raporunda patates kromozomunda resesif öldürücü bir alelin genetik kanıtı. Am. J. Patates Arş. 96, 331 (2019).
- 21. van Lieshout, N. ve ark. Patates (Solanum tuberosum) için yeni oldukça bitişik referans genomu Solyntus. G3 Genleri Genomları Genet. 103489-3495 (2020).
- 22. Leisner, CP ve diğerleri. Yüksek glikoalkaloid üreten yumrulu patates türlerinin diploid kendilenmiş bir klonu olan M6'nın genom dizisi Solanum chacoense, artık heterozigotluğu ortaya çıkarır. Bitki J. 1967562-570 (2018).
- 23. Peterson, BA ve diğerleri. Yetiştirilmiş bir diploid patates popülasyonunda kendi kendine doğurganlık, infinium 8303 patates tek nükleotid polimorfizm dizisi ile incelendi. Bitki Genomu https://doi.org/10.3835/plantgenome2016.01.0003 (2016).
- 24. Lian, Q. ve diğerleri. Patates poliploidizasyonu sırasında zararlı mutasyonların kazanılması. J. Integr. Bitki Biol. 617-11 (2019).
- 25. van Lieshout, N. ve ark. Patates için son derece bitişik yeni referans genomu Solyntus (Solanum tuberosum). G3 Genleri Genomları Genet. 631911, g3.401550.2020 (2020).
- 26. Van Ooijen, JW KatılınHarita®4, Deneysel Popülasyonlarda Genetik Bağlantı Haritalarının Hesaplanmasına Yönelik Yazılım Cilt 33 (Kyazma BV, 2006).
- 27. van Ooijen, JW Otogam türlerde niceliksel özellik lokuslarının haritalanmasının doğruluğu. Teori. Appl Genet. 84803-811 (1992).
- 28. Voorrips, RE Mapchart: bağlantı haritalarının ve QTL'lerin grafiksel sunumu için yazılım. J. Hered. 9377-78 (2002).
- 29. Hirsch, CD ve diğerleri. Spud DB: patates yetiştiriciliğini hızlandırmak için madencilik dizileri, genotipler ve fenotipler için bir kaynak. Bitki Genomu. 7, https://doi.org/ 10.3835/bitki genomu2013.12.0042 (2014).
- 30. Bankevich, A. ve diğerleri. SPAdes: yeni bir genom birleştirme algoritması ve bunun tek hücreli dizilemeye uygulamaları. J. Bilgisayar. Biyol. 19455-477 (2012).
- 31. Sharma, SK ve diğerleri. Patates için referans kromozom ölçekli psödomoleküllerin oluşturulması: patates genomunun genetik ve fiziksel haritalarla bütünleştirilmesi. G3 Genleri Genomları Genet. 32031-2047 (2013).
- 32. Fernandez-Pozo, N. ve diğerleri. Sol Genomik Ağı (SGN) - genotipten fenotipe ve üremeye. Nükleik Asitler Arş. 43, D1036-D1041 (2015).
- 33. Kim, S. ve diğerleri. Acı biberin genom dizisi, keskinliğin evrimi hakkında fikir verir. Kırmızı biber türler. Nat. Genet. 46270-278 (2014).
- 34. Santillan Martinez, MI ve diğerleri. Küllemeye karşı direnç için domates duyarlılık geni PMR9'ün CRISPR/Cas4 hedefli mutajenezi. BMC Bitki Biol. 201-13 (2020).
- 35. Liang, G., Zhang, H., Lou, D. ve Yu, D. CRISPR/Cas9 tabanlı bitki genom düzenlemesi için yüksek verimli sgRNA'ların seçimi. Sci. Cum. 61-8 (2016).
- 36. Stemmer, M., Thumberger, T., Del Sol Keyer, M., Wittbrodt, J. & Mateo, JL CCTop: sezgisel, esnek ve güvenilir bir CRISPR/Cas9 hedef tahmin aracı. PLoS ONE 10,1-11 (2015).
- 37. Zuker, M. Nükleik asit katlanması ve hibridizasyon tahmini için Mfold web sunucusu. Nükleik Asitler Arş. 313406-3415 (2003).
- 38. Chari, R., Yeo, NC, Chavez, A. & Church, GM SgRNA Scorer 2.0: CRISPR/Cas9 aktivitesini tahmin etmek için türden bağımsız bir model. ACS Sentezi. Biol. 6902-904 (2017).
- 39. Visser, RGF in Bitki Doku Kültürü Kılavuzu 301-309 (Springer, 1991).
Rekabet ilgi
Yazarlar, hiçbir çıkar çatışması olmadığını beyan eder.
Ek bilgi
Ek bilgi Çevrimiçi sürüm şu adreste bulunan ek materyali içerir: https://doi.org/10.1038/s41467-021-24267-6.
Yazışma ve malzeme talepleri CWBB'ye iletilmelidir.
Meslektaş incelemesi bilgileri Doğa İletişim Roger Chetelat'a ve diğer anonim hakem(ler)e bu çalışmanın hakem değerlendirmesine yaptıkları katkılardan dolayı teşekkür ederiz. akran değerlendirme raporları mevcuttur.
Yeniden basımlar ve izin bilgileri mevcuttur http://www.nature.com/reprints
Publisher'not Springer Nature yayımlanmış haritalar ve kurumsal bağlamlarda yargılama iddialarına karşı tarafsız kalmaktadır.
Teşekkür
pAGM:CRISPRASli ile iki patates genotipinin dönüşümünde Veronica Tammy Soputro'ya, BSc ve MSc öğrencileri Gilo Pleunis, Iris Smits, Niki Vorgia, Hidde Knuiman, Maurice Geurts, Anja van Heteren ve Torsten van der'e yardımlarından dolayı teşekkür ederiz. Haritalama popülasyonlarının fenotiplenmesindeki yardımları için Schriek'e ve RNA örnekleri oluşturma konusunda Tess Lucas'a teşekkür ederiz. Ayrıca Solynta ve Wageningen Üniversitesi Unifarm sera çalışanlarına bitkilerin bakımı ve tohum çıkarma konusundaki yardımlarından dolayı teşekkür ederiz. Bu proje Hollanda Bilimsel Araştırma Örgütü'nden mali destek almıştır (Grant ID: NWA.17.023).
Yazar Katkıları
E.-JE deneyleri tasarladı, yürüttü ve taslağı yazdı. AvdB, WGS, KASP işaretçisi ve biyoinformatik yaklaşımlarını tasarladı ve uyguladı. SvH, RGFV, CWBB, MEdV ve PL, genetik haritalama çalışmaları ve fonksiyonel karakterizasyonu için yaklaşımın tasarlanmasına yardımcı oldu. sli. RGFV, CWBB ve PL taslağı gözden geçirdi ve yorum yaptı.
ben(S)Q) Access'i açın Bu makale, orijinal yazarlara ve kaynaklara uygun kredi verdiğiniz sürece, herhangi bir ortamda veya biçimde kullanım, paylaşım, uyarlama, dağıtım ve çoğaltmaya izin veren Creative Commons Atıf 4.0 Uluslararası Lisansı kapsamında lisanslanmıştır. Creative Commons lisansına bağlanın ve değişikliklerin yapılıp yapılmadığını belirtin. Bu makaledeki resimler veya diğer üçüncü taraf materyaller, materyale ilişkin bir kredi satırında aksi belirtilmedikçe, makalenin Creative Commons lisansına dahildir. Materyal, makalenin Creative Commons lisansına dahil değilse ve kullanımınıza yasal düzenlemeler tarafından izin verilmiyorsa veya izin verilen kullanımı aşmıyorsa, doğrudan telif hakkı sahibinden izin almanız gerekir. Bu lisansın bir kopyasını görüntülemek için şu adresi ziyaret edin: http://creativecommons.org/ lisanslar/by/4.0/.









